Già il 24 agosto 2021, Cara Therapeutics e il suo partner commerciale Vifor Pharma hanno annunciato che il suo agonista del recettore degli oppioidi kappa, difelikefalin (KORSUVA™), primo nella sua classe, era stato approvato dalla FDA per il trattamento dei pazienti con malattia renale cronica (MRC) (prurito moderato/grave positivo in trattamento emodialitico); il suo lancio è previsto per il primo trimestre del 2022. Cara e Vifor hanno firmato un accordo di licenza esclusiva per la commercializzazione di KORSUVA™ negli Stati Uniti e hanno concordato di vendere KORSUVA™ a Fresenius Medical. Cara e Vifor detengono ciascuna una quota di profitto del 60% e del 40% sul fatturato di aziende diverse da Fresenius Medical; ciascuna detiene una quota di profitto del 50% sul fatturato di Fresenius Medical.
Il prurito associato a CKD (CKD-aP) è un prurito generalizzato che si manifesta con elevata frequenza e intensità nei pazienti con CKD sottoposti a dialisi. Il prurito si manifesta in circa il 60-70% dei pazienti sottoposti a dialisi, di cui il 30-40% presenta prurito moderato/grave, che influisce gravemente sulla qualità della vita (ad esempio, scarsa qualità del sonno) ed è associato a depressione. Non esisteva finora alcun trattamento efficace per il prurito correlato a CKD e l'approvazione di Difelikefalin contribuisce a colmare l'enorme lacuna nella domanda di autorizzazione all'immissione in commercio. Questa approvazione si basa su due studi clinici pivotali di Fase III in fase di deposito per la NDA: dati positivi dagli studi KALM-1 e KALM-2 negli Stati Uniti e a livello globale, e dati di supporto da 32 ulteriori studi clinici, che dimostrano la buona tollerabilità di KORSUVA™.
Non molto tempo fa, sono arrivate buone notizie dallo studio clinico sulla difelikefalin in Giappone: il 10 gennaio 2022, Cara ha annunciato che i suoi partner Maruishi Pharma e Kissey Pharma hanno confermato che l'iniezione di difelikefalin è utilizzata in Giappone per il trattamento del prurito nei pazienti in emodialisi. Studi clinici di fase III L'endpoint primario è stato raggiunto. 178 pazienti hanno ricevuto 6 settimane di difelikefalin o placebo e hanno partecipato a uno studio di estensione in aperto di 52 settimane. L'endpoint primario (variazione del punteggio della scala di valutazione numerica del prurito) e l'endpoint secondario (variazione del punteggio del prurito sulla scala di gravità Shiratori) sono migliorati significativamente rispetto al basale nel gruppo difelikefalin rispetto al gruppo placebo e sono stati ben tollerati.
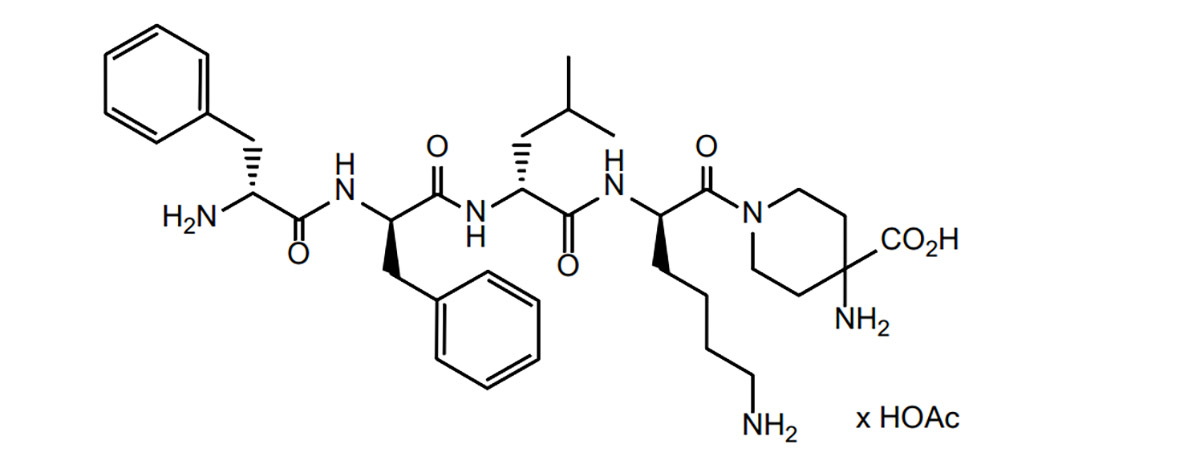
La difelikefalina è una classe di peptidi oppioidi. Sulla base di ciò, il Peptide Research Institute ha studiato la letteratura sui peptidi oppioidi e ha riassunto le difficoltà e le strategie dei peptidi oppioidi nello sviluppo di farmaci, nonché l'attuale situazione dello sviluppo di farmaci.
Data di pubblicazione: 17-02-2022